形状记忆合金(shape memory alloys,SMA)是一类具有在热机械变形或磁变形等特定刺激作用下保持预编程形状能力的形状记忆材料[1]。自1932 年 SMA被发现后,已发现几十种不同的合金材料具有形状记忆效应,可概括为镍钛(NiTi)合金、铁基合金、镁基合金和铜基合金[2]。由于具有优异的生物相容性[3]、稳定性[4]和热机械性能,以 NiTi合金(nickel-titanium alloy或 Ni-Ti alloy)为基础的 SMA在大多数应用中更为可取,如航空航天、骨科植入物和固定装置、联接器和紧固件、电气安全装置、海军、运动设备以及外科手术器械等[5-6]。
然而,由于镍钛合金中含镍量达50 at%左右,一旦植入体发生腐蚀,镍离子(Ni2+)就会溶出向四周扩散导致细胞畸变,甚至产生癌变作用,影响其本身性能,从而限制了它在医学领域的长期使用[7]。为此,国内外学者尝试做了大量的表面处理,采用物理化学、电化学、形态学及生物化学等多种方法对镍钛记忆合金表面进行改性,如等离子喷涂
[8]、离子注入[9]、电解抛光[10]、阳极氧化[11]、酸碱处理[12]等,这些技术均在不同程度上取得了良好的效果,但都有各自的不足之处。孙向东等[13]研究指出,镍钛合金去合金化的实现途径有两种:一是降低去合金液内的镍离子浓度;二是在表面形成稳定的钛氧化物。因此本研究选用强氧化剂过氧化氢溶液对镍钛合金进行处理,旨在确保其生物安全性的同时,能在镍钛合金表面形成稳定的氧化物。
本研究将对3D打印镍钛合金进行去合金化处理并与酸蚀处理对比,研究其理化特征、成骨活性功能,旨在探究一种更加简便、高效的表面处理方式,以保障其安全性,并提升它的耐腐蚀能力及生物性能,为镍钛合金作为医用材料特别是植入 /介入器械的长期安全临床应用,提供可借鉴的思路和理论指导。
一、材料与方法
1、主要材料及试剂、仪器:
镍钛合金粉末(德普润新材料,北京);人骨髓间充质干细胞(human bone marrow mesenchymalstem cells,hBMSCs)(佳木斯大学基础医学院提供);过氧化氢溶液(大茂化学试剂,天津);盐酸溶液(欧博凯化工,天津);硫酸溶液(欧博凯化工,天津);MEM培养基(Biosharp,上海);胎牛血清(Gibco,美国);CCK-8 细胞检测试剂盒(Beyotime,上海);Mlab 3D打印机(GE Additve,美国);FV1000 激光共聚焦显微镜(Olympus,日本);JC200001 接触角测量仪(中晨设备,上海);RS232 多功能酶标仪(麦莎生物,上海)。
2、实验分组及方法:
使用 Geomagic Design X软件进行设计建模,镍钛试件尺寸设计为直径10 mm、厚度为2 mm的圆片,将数据导入3D打印机中,选择镍钛合金打印参数进行打印,本实验使用的镍钛合金粉末为平均粒径10~53 μm的球形近等原子比粉末。
A组:使用150 目 Al2O3 砂砾,喷砂角度为90°,压强为0.2 MPa,时间60 秒,对样品进行喷砂处理。
B组:将以上喷砂后的试样放入70℃的盐酸与硫酸(浓度比例1:1)溶液中酸蚀处理60 分钟。
C组:将喷砂处理后的试样置于80℃浓度为15%、pH为3 的过氧化氢溶液中3 小时,进行去合金处理。
3、 观测指标:
(1)表面理化性能表征:
每 组 各 取1 个 样 品, 用 扫 描 电 子 显 微 镜(scanning electron microscope, SEM) 观 察 表 面形貌特征;每组取3 个样品,用能谱仪(energydispersive spectrometer, EDS)对各组表面成分进行分析,测量后取均值;室温下用接触角测量仪测量表面接触角。
(2)体外细胞相容性评价:
①细胞培养48 小时后每组各取1 个样品,处理后加入鬼笔环肽与赫斯特细胞核蓝色荧光染料(Hoechst 33342)分别进行细胞骨架和细胞核染色,然后利用激光共聚焦扫描显微镜(laserscanning confocal microscope, LSCM)对细胞位置和蛋白骨架进行观察。每组取3 个样品置于24孔板中,每孔加入3×104 个 hBMSCs 悬液500 μL与试样共培养,置于37℃、5% CO2 培养箱培养1、3、5 天后,每组5 个复孔,用 CCK-8 试剂盒进行检测。②在灭菌后的试样表面以2×104 个细胞 /每孔接种,并用完全培养基培养,3 天后换 成诱导培养基培养,隔天更换1 次培养基,采用天狼星红染色方法测定 I型胶原分泌情况。③茜素红染色法测定细胞外基质的矿化程度。
4、 统计学方法:
采用 Graphpad Prism 8 进行统计分析,实验结果采用平均值 ±标准差表示,如果 P<0.05,则认为差异具有统计学显著性。
二、实验结果
1、 表面理化性能表征:
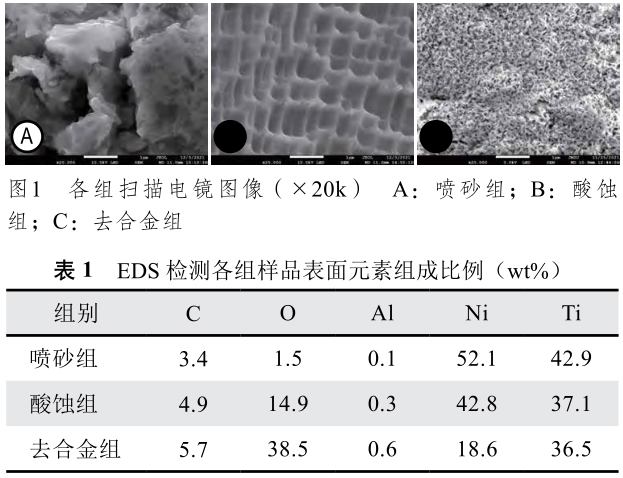
SEM结果显示喷砂组表面呈形状不规则的凹坑和冲击痕;酸蚀组形成类似纤维网格状的结构;去合金组表面获得了均匀、多孔的纳米网架结构(图1)。
EDS结果如表1,去合金后表面镍元素(Ni)含量比其他两组明显降低,为18.6 wt%,氧元素(O)含量也较其他两组高。
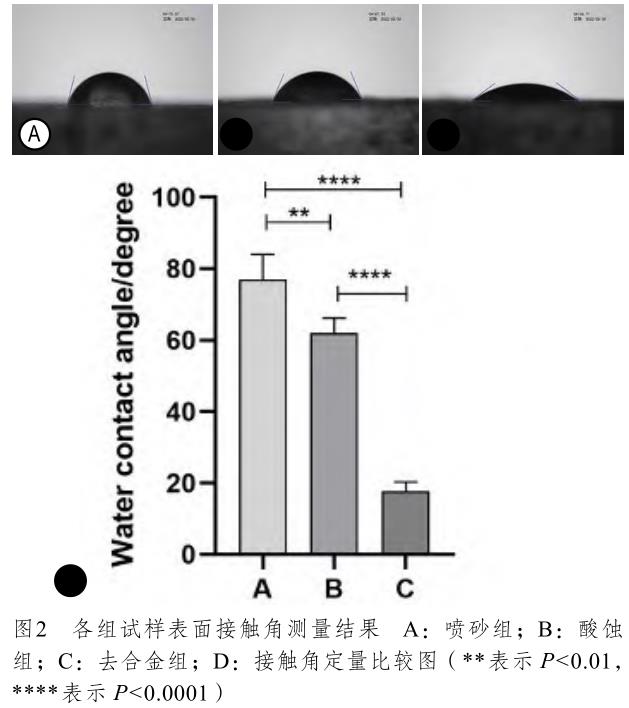
接触角测量仪检测结果如图2,喷砂组、酸蚀组和去合金组的表面水接触角分别为76.99°±7.03°、62.05°±4.14°和17.67°±2.66°,组间比较差异均有统计学意义(P<0.01)。
2、体外细胞相容性评价:
(1)细胞形态观察:
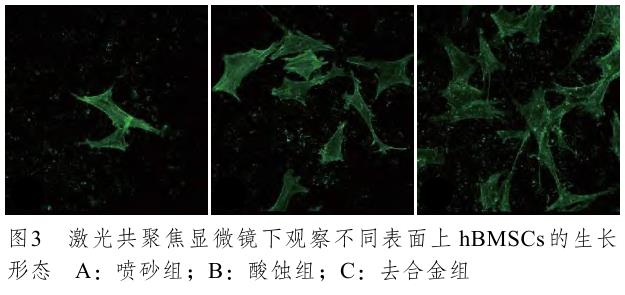
图3 所示,在喷砂处理后,表面上 hBMSCs数量较少且未见到伪足生长,也无明显的铺展;在酸蚀处理组试样的表面,细胞的生长形态相似,伪足增多,向四周铺展,细胞数量也有所增加;在去合金组的试样表面,所有细胞都铺展良好,覆盖的面积也较其他组增大,并且向三维方向伸展,伪足和胞间连丝都增加,细胞之间已没有了界限。
(2)细胞增殖实验:
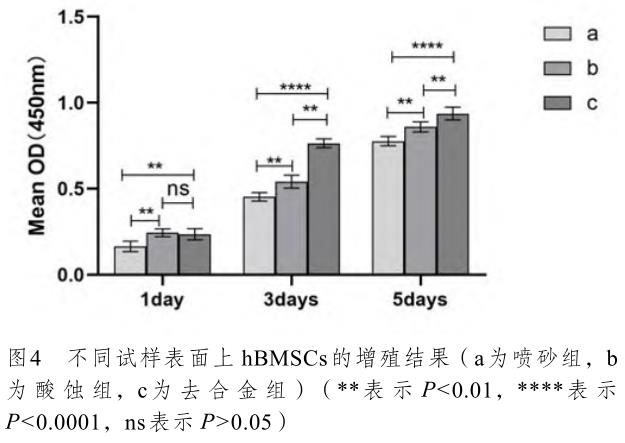
CCK-8 细胞增殖实验检测结果显示,培养1、3、5 天后,各组细胞的生长速度随着培养时间的延长呈递增趋势,不同时间点的比较有显著性差异(P<0.05)。实验结果证明,去合金组试样表面的细胞增殖最快,酸蚀组次之,喷砂组最慢(图4)。
(3)细胞分化能力检测:
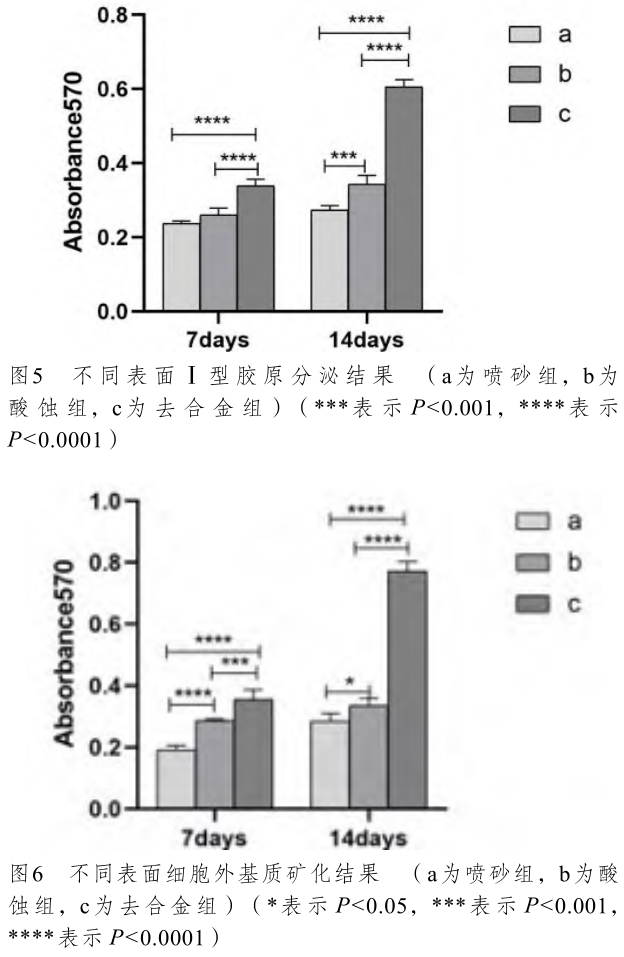
图5、图6 分别是不同样品表面诱导细胞培养7 天和14 天后Ⅰ型胶原分泌与细胞外基质矿化的结果,随着诱导时间延长,去合金组的Ⅰ型胶原和细胞外基质矿化水平增加最多,增长速度也较其他组更快,说明去合金化处理能够促进 hBMSCs分化,且随着诱导时间延长,对hBMSCs分化的促进作用更明显。
三、讨论
作为植入材料,未经处理的3D打印镍钛合金表面由于较粗糙,没有微孔结构,不利于细胞的识别和黏附,且其在接触体液时,因为腐蚀可能导致植入体镍离子的释放,可能会对人体产生毒性[14-15],因此必须不断通过各种表面处理方法提高镍钛合金植入物的理化特性,从而增强植入物的生物学性能,提高生物相容性,促进植入体与骨组织的结合,缩短愈合时间。去合金是一种以化学或电化学的方式,对一种或几种金属进行选择性的蚀刻,然后用不同材料之间的电势差异,将一种以上的活性金属离子进行选择性的溶解,以获得具有连续的十纳米到几百微米的三维孔隙结构[16]。目前,去合金法由于其经济、高效、可控等优点在纳米多孔体的制造中得到了越来越多的重视,但目前国内对镍钛合金去合金的相关报道较少,且去合金后的镍钛合金生物相容性有待进一步检验。
本研究中去合金处理后的表面较其他两组形成更加丰富的纳米级网架结构,说明它可以使喷砂后的不规则表面产生多级孔隙,也因此可以消除喷砂后表面形成的不规则浅坑,而且相较于酸蚀后的表面,去合金可以使表面孔洞加深、数量增多,排列也更紧密,为表面亲水性能提供了形貌基础。本实验结果可见,与其他两组相比,去合金表面的镍元素含量降至18.6 wt%,大大降低了镍离子释放对人体产生毒性的可能;在去合金组,氧元素的含量也明显增加,表明其对金属的氧化有一定促进作用,在其表面可能形成亲水性的氧化钛膜层[17]。
理想的植入体应具有良好的细胞相容性和良好的成骨活性。本研究在去合金化的过程中,表面增加了纳米级网格结构,为细胞的附着和延伸创造了更多空间,从而使其更多地向三维方向延伸,而围绕着网格突起的边缘也“锚定”了由细胞延伸出来的伪足,并且与试件接触更加紧密。表明随着植入体润湿性的增大,其扩展区域也随之增大[18]。Hallab等[19]的实验还表明,植入体的表面与亲水性的关系比,表面粗糙度对其影响更明显。从体外细胞活性实验可以看出,各组样品都支持细胞的增殖与分化,随着植入体浸润性的增强,其细胞增殖能力和骨结合能力也随之增强[20],同时也说明骨髓间充质干细胞能够承受样品释放的 Ni2+,有研究也证明等原子比镍钛合金对细胞具有极低的毒性,表明其具有良好的生物相容性[21]。
本研究中去合金化形成的纳米级网格状结构表面是一种良好的表面改性方法,优化了试件的表面性能,具有良好的细胞相容性,并且能够促进成骨功能的表达,有望改善镍钛植入物的骨结合能力和植入物的长期稳定,但其在体内的相关指标验证还需进一步通过动物实验来实现。
利益冲突 本文作者均声明不存在利益冲突作者贡献声明 秦欣玉:实验设计、实验实施、数据分析和论文写作等全过程;张亮、陈莹莹、韩泽奎:参与实验实施;宿玉成、王心彧:提供研究经费、论文修改和审阅指导。
参考文献
[1]Mohd Jani J, Leary M, Subic A, et al. A review of shape memory alloy research, applications and opportunities[J].Materials and Design, 2014,56:1078-1113.DOI:10.1016/j.matdes.2013. 11.084
[2]谭树松 . 形状记忆合金研究的最新进展及应用 [J]. 功能材料 ,1991,3:185-190,192.
[3]Patel S K, Behera B, Swain B, et al. A review on NiTi alloys for biomedical applications and their biocompatibility[J].Materials Today: Proceedings, 2020,33:5548-5551.DOI:10.1016/j.matpr. 2020.03.538.
[4]Mani G, Porter D, Grove K, et al. Surface finishing of nitinol for implantable medical devices: a review[J]. JBiomed Mater Res B Appl Biomater, 2022,110(12):2763- 2778. DOI: 10.1002/jbm.b.35112.
[5]Nair VS, Nachimuthu R. The role of NiTi shapememory alloys in quality of life improvement through medical advancements: a comprehensive review[J].
Proc Inst Mech Eng H, 2022,236(7):923-950. DOI:10.1177/09544119221093460.
[6] Bhagyaraj J, Ramaiah K V, Saikrishna C N, et al. Behavior and effect of Ti2Ni phase during processing of NiTi shape memory alloy wire from cast ingot[J].Journal of Alloys andCompounds , 2013,581:344-351.
[7]Močnik P, Kosec T. A critical appraisal of the use and properties of nickel-titanium dental alloys[J]. Materials (Basel), 2021,14(24):7859. DOI: 10.3390/ma14247859.
[8] Bogdanski D, Epple M, Esenwein S A, et al.Biocompatibility of calcium phosphate-coated and of geometrically structured nickel–titanium (NiTi) by in vitro testing methods[J]. Materials Science & Engineering.A, Structural Materials : Properties, Microstructure and Processing, 2004,378(1): 527-531. DOI:10.1016/ j.msea.2003.11.071
[9]Wu SL, Chu PK, Liu XM, et al. Surface characteristics,mechanical properties, and cytocompatibility of oxygen plasma-implanted porous nickel titanium shape memory alloy[J]. J Biomed Mater Res A, 2006,79(1):139-146. DOI:10.1002/jbm.a.30705.
[10]Kim J, Park JK, Kim HK, et al. Optimization of electropolishing on NiTi alloy stents and its influence on corrosion behavior[J]. J Nanosci Nanotechnol, 2017,17(4):2333-2339. DOI: 10.1166/jnn.2017.13324.
[11]Mohammadi F, Golafshan N, Kharaziha M, et al. Chitosan-heparin nanoparticle coating on anodized NiTi for improvement of blood compatibility and biocompatibility[J].Int J Biol Macromol, 2019,127:159-168. DOI: 10.1016/j.ijbiomac.2019.01.026.
[12]Lee SY, Lee CH, Kim DY, et al. Preparation and photocatalytic activity of potassium- incorporated titanium oxide nanostructures produced by the wet corrosion process using various titanium alloys[J]. Nanomaterials (Basel),2015,5(3):1397-1417. DOI: 10.3390/nano5031397.
[13]苏向东 , 王天民 , 郝维昌 , 等 . 低温去合金化处理对医用镍钛合金表面性质的影响 [J]. 稀有金属材料与工程 ,2008,37(5):859-863. DOI: 10.3321/j.issn:1002-185X.2008. 05.026.
[14]Pound BG. The electrochemical behavior of nitinol in simulated gastric fluid[J]. J Biomed Mater Res B Appl Biomater, 2017,105(8):2394-2400. DOI: 10.1002/jbm. b.33779.
[15]Pound BG. Corrosion behavior of nitinol in blood serum and PBS containing amino acids[J]. J Biomed Mater Res B Appl Biomater, 2010,94(2):287-295. DOI: 10.1002/jbm.b.31647.
[16] Song T, Gao Y, Zhang Z, et al. Dealloying behavior of rapidly solidified Al–Ag alloys to prepare nanoporous Ag in inorganic and organic acidic media[J]. CrystEng Comm,2011,13:7058-7067. DOI:10.1039/c1ce05538k.
[17]崔跃 , 张宝祥 , 马连彩 , 等 . 镍钛合金在医疗器械领域应用和表面改性研究进展 [J]. 材料导报 ,2017, 31(z2):197-200.
[18]Bacakova L, Filova E, Parizek M, et al. Modulation of cell adhesion, proliferation and differentiation o n m a t e r i a l s d e s i g n e d f o r b o d y i m p l a n t s [ J ] .Biotechnol Adv, 2011,29(6):739-767. DOI: 10.1016/j.biotechadv.2011.06.004.
[19]Hallab NJ, Bundy KJ, O'Connor K, et al. Evaluation of metallic and polymeric biomaterial surface energy and surface roughness characteristics for directed cell adhesion[J]. Tissue Eng, 2001,7(1):55-71. DOI:10.1089/107632700300003297.
[20]Rupp F, Liang L, Geis-Gerstorfer J, et al. Surface characteristics of dental implants: a review[J]. Dent Mater,2018,34(1):40-57. DOI: 10.1016/j.dental.2017.09.007.
[21]Alipour S, Taromian F, Ghomi ER, et al. Nitinol: from historical milestones to functional properties and biomedical applications[J]. Proc Inst Mech Eng H, 2022,236(11):1595-1612. DOI: 10.1177/09544119221123176.
无相关信息


yongyiti.com
永益钛手机网